お客様へのご提案
課題
- 滅菌注射剤の包装工程における汚染により、1年間の廃棄バッチ数が2桁に上っていた。
ソリューション
- 製造インテリジェンス - FactoryTalkソフトウェアアプリケーションが制御システムからのデータを保存および整理、表示し、FDAに提出するレポートを自動作成およびカスタマイズするとともに、品質管理を徹底
- 製造インテリジェンス - オートメーテッド・システムズ社が、業界に関する専門知識とシステム設計、構成、実装、検証、プロジェクト管理を一括して提供
結果
- バッチの廃棄をゼロにすることで、少なくとも年間25万ドルの節約を達成
- 監視レベルでのリモート・バッチ・ステータス・モニタにより、1人のオペレータが複数のプロセスを担当可能
- レポートがPDF形式で保存され、バッチのトレーサビリティが実現
- 履歴データを活用して、トレンド分析やプロセス分析が可能
- ロールベースの主要業績評価指標(KPI)に沿って構成されたダッシュボードレポートが、オペレータやマネージャに明確で実用的なリアルタイムの情報を提供
背景米国では、命にかかわる医薬品の多くが供給不足に陥っており、患者たちはこれに猛抗議し、議会聴聞会まで開かれたほどです。なかでも切実に必要とされているのが、注射または点滴で静脈内投与される液剤です。現に、連邦食品医薬品局(FDA)の不足品目リストに挙げられている薬剤の75%近くが、化学療法薬や麻酔薬、栄養剤などの液剤となっています。
医薬品の生産においては、製品の純度維持のため所定のプロセスが厳格に義務付けられていますが、FDAと業界専門家の間では、そのプロセスの複雑さが問題の大きな要因であるという点で見解が一致しています。2010年単独で見ても、製薬会社が生産した注射剤の半数以上のバッチが、細菌汚染や不純微粒子の混入など、品質上の問題によって廃棄されています。
ここで、ある製造メーカの事例をご紹介します。これは状況の深刻さを物語ると同時に、オートメーション技術を活用していかにそれを克服できるかを示す事例でもあります。
課題
米国を本拠地とするこの滅菌注射剤メーカでは、包装ライン上の汚染による1年間の廃棄バッチ数が2桁に上っていました。このプロセスにおける問題は、成形同時充填(BFS)機を使用してバルク容器から個々のプラスチック製バイアルに薬剤を移す際に発生していました。
すべての機器が無菌状態にあることを確認するため、薬剤を投入する前に、プロセス全体に20~30個存在するバルブをオペレータが開閉して手作業でラインに圧力を加えます。これによって外気は遮断され、汚染物質が排除されます。しかし、バルブを開く順序やタイミングを誤ると、バッチに汚染が生じる可能性があります。
また、人為的エラー以外にも問題がありました。バルブの密閉機能や機器のカップリングの欠陥によっても圧力損失が生じ、製品の純度が低下することがあるのです。また、ラインには潜在的な障害を通知するアラームシステムが存在しなかったため、プラントのオペレータは、バッチに問題があったかどうかを完成品のテストが行なわれるまで知ることができませんでした。
ソリューション
この製薬会社は包括的なソリューションを求め、制御・視覚化システムのアップグレードをオートメーテッド・システムズ(ASI)社に依頼しました。そこでASI社が構築したシステムは、ライン上の汚染を自動的に食い止め、プロセス上の何らかの要素が指定範囲を逸脱した場合にはアラームを発するほか、主なプロセスデータを追跡・記録することにより、完了した各バッチの無菌状態を確認できるものでした。
このソリューションの核となったのが、ロックウェル・オートメーションのハードウェアおよびソフトウェアを基盤に据えた製造インテリジェンス戦略です。ASI社のエンジニアは、新しいAllen-Bradley®のControlLogix®プログラマブル・オートメーション・コントローラを活用して、重要な鍵を握る加圧手順を含め、各種処理やシーケンシングの全手順を事前に設定できるシステムを設計しました。
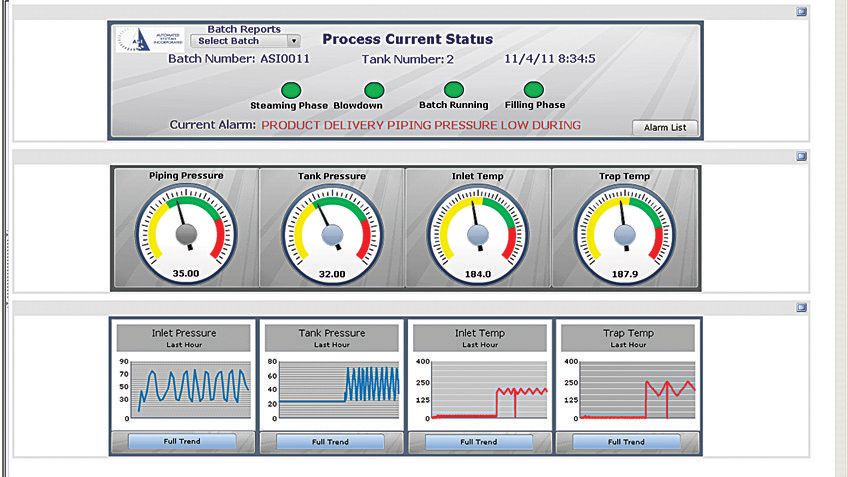
このシステムはロックウェル・オートメーションのFactoryTalkソフトウェアを採用しており、これにはFactoryTalk® View Site Edition (SE)ソフトウェアを実行するヒューマン・マシン・インターフェイス(HMI)が含まれます。このHMIは、システムの状態をリアルタイムで高度な模擬画面に表示します。この画面にはセキュアなWebブラウザからもアクセスできるため、オペレータはこれを活用してリモートモニタを行ない、システム内のすべてのバルブの状態と圧力や温度の測定値を詳細に確認できます。
つまり、システムの状態を隅々まで把握したうえで、適切な操作を迅速かつ正確に実行できるのです。FactoryTalk View SEソフトウェアは、所定の操作を実行してプロセスの各手順における異変を確認するよう、プロンプトを表示します。警告やアラームが発動されると、システムが潜在的な障害箇所を自動的に特定し、そのエリアの製品を隔離してラインを再滅菌します。
また、記録管理の改善およびレポート作成の簡易化を目指し、ASI社はこの新システムにFactoryTalk HistorianおよびVantagePoint EMIソフトウェアを組み込みました。これらのアプリケーションは互いに連携し、重要なプロセスパラメータおよびアラームをすべて追跡・記録します。オペレータは自動生成されたインターフェイスやダッシュボード、レポートを通じて重要な生産データにリアルタイムでアクセスできるため、生産上の潜在的な問題を発生前に解決できます。その一方で、事業部マネージャは履歴データの評価を行ない、より豊富な情報に基づいて意思決定を下すことができます。
各運転サイクルの終了時にはレポートが自動生成され、アラームや無菌状態に影響を及ぼす状況がリストされます。何らかの異常が見られた場合、オペレータは履歴データを参照してエラーの発生箇所を正確に特定し、素早く状況を是正できます。また、生産データは自動追跡されるため、プロセスの終了後に各バッチをテストする必要もありません。
レポートはPDF形式で保存され、これによってバッチのトレーサビリティも実現しています。プラントのオペレータおよびマネージャは、履歴データを活用してトレンド分析やプロセス分析を実施できます。
さらに、FactoryTalk HistorianおよびVantagePoint EMIソフトウェアにより、規制によるレポート要件も満たすことができます。FactoryTalk Historianは記録の安全なリポジトリとして機能し、製造メーカはこれを活用して、電子記録に関するFDAの規則を遵守できます。FactoryTalk VantagePoint EMIは、システムが信頼できる補足データをバッチ記録と関連付け、医薬品適正製造基準へのコンプライアンスを強化するのに役立ちます。
結果
新システムの導入以来、この製造メーカにおいて汚染によるバッチ廃棄は1件も発生していません。完了した各バッチには25万ドル以上の価値があるため、新システムへの投資は早くも元がとれたことになります。
また、新システムはバッチの安全性を自動追跡するため、FDAへのレポートに関する規制遵守に費やす時間と資金も削減されました。
患者にも、必要な薬剤の供給という便益がもたらされています。
公開 2015年5月28日